随着全球减重药物竞争进入白热化阶段,单一的GLP-1受体激动剂已不再是唯一“战场”,行业正加速向多靶点协同、给药方式革新以及长效化体重管理的“2.0时代”跃迁。作为国内GLP-1类药物重要参与者,博瑞医药(688166.SH)如何应对?1月30日晚,公司在最新发布的公告中,罕见地披露并更新了多项处于临床前及PCC阶段的创新减重管线,进一步拓展了其在代谢疾病领域的技术纵深,引发业界关注。
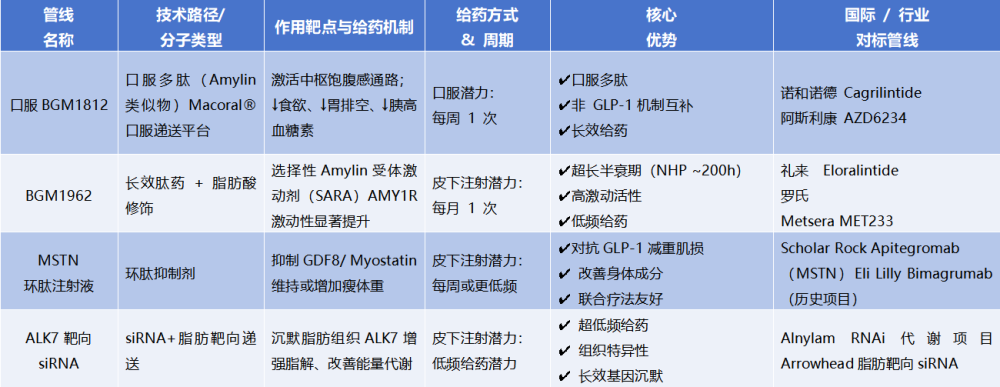
据披露内容显示,相关新增管线不仅涵盖基于Amylin通路的口服与长效注射制剂,也前瞻性布局了瘦体重保护及脂肪组织代谢调控等关键方向,包括最新进展的口服多肽制剂BGM1812、长效选择性胰岛淀粉样肽受体激动剂BGM1962,以及用于维持瘦体重的MSTN环肽注射液和具备超低频给药潜力的ALK7靶向siRNA项目。
业内人士指出,这些管线在作用机制、给药周期及联合应用潜力上形成清晰分工,标志着公司减重药物布局已由单一产品推进,升级为系统化、多层次的产品组合。从颠覆性的口服多肽制剂到跨代的 siRNA基因沉默技术,博瑞医药正以“第一梯队”姿态,在全球范围内构建差异化的代谢疾病治疗版图。博瑞医药在对标国际制药巨头的正面竞争中展现出显著的爆发潜力,预示着中国创新药企正从全球规则的“追随者”,逐步迈向代谢赛道的“定义者”。
多靶点协同:从“减重”向“健康减重”的范式转移
在全球减重药研发的下半场,如何解决“瘦体重(肌肉)流失”已成为诺和诺德、礼来等跨国巨头共同攻克的难题。医学界日益达成共识:高质量的减重不应以牺牲肌肉量为代价,因为肌肉流失会导致基础代谢率下降,进而引发更严重的“反弹”效应,甚至导致肌少症风险。博瑞医药披露的MSTN环肽注射液,正是针对这一痛点的精准创新。本产品目前处于PCC(临床前候选化合物)阶段。
该产品作为公司自主研发的高选择性肌生成抑制素(GDF8)环肽抑制剂,旨在与减重疗法(如GLP-1/GIP双重激动剂BGM0504)联用,在强效减脂的同时“锁定”肌肉量,从而改善身体成分、促进更健康的体重管理。
在临床前研究中,该产品在有效减重的同时能显著维持瘦体重,从而改善身体成分。这一布局直接对标礼来(Eli Lilly)通过收购Versanis获得的单克隆抗体Bimagrumab。与国际巨头采用的抗体路径相比,博瑞医药选择的环肽路径在生产工艺简化与靶向灵活性上具备独特潜力。MSTN环肽在大鼠中表现出23.9小时的良好半衰期,支持每周或更低频次的给药方案。这种“减重+保肌”的组合拳,不仅能提升患者的体能表现与代谢健康,更标志着博瑞医药已步入代谢病精准治疗的前沿,致力于定义“高质量减重”的新标准。
长效与口服:挑战依从性的天花板
依从性是减重药商业化的核心维度,博瑞医药在给药便利性上正不断挑战行业天花板,旨在将减重从一种“医疗负担”转变为“生活方式”。
公司开发的口服BGM1812,是优化设计的新型长效Amylin类似物。Amylin(胰淀素)作为饱腹感信号的天然传导者,能通过激活大脑中枢通路精准抑制食欲并延缓胃排空,这种非GLP-1依赖的机制能有效避免传统药物常见的消化道副作用。该靶点直接对标诺和诺德(Novo Nordisk)的重磅在研药物CagriSema中的Cagrilintide组分。
借力Macoral®口服多肽制剂平台,BGM1812成功克服了多肽在消化道内极易降解的难题,具备每周给药一次的潜力。这不仅有望打破多肽药物必须依赖注射的行业瓶颈,更意味着患者可以像服用普通维他命一样轻松管理体重,大幅提升了用药的便利性。
与此同时,公司另一款长效选择性胰岛淀粉样肽受体激动剂(SARA)BGM1962,则通过精密的肽序列优化与脂肪酸修饰技术,挑战了生物药给药频次的物理极限。该产品在长效化维度上可对标安进(Amgen)处于临床阶段的每月一次给药方案。本产品目前处于临床前研究阶段。
在药物研发中,半衰期的每一次延长都代表着分子结构的质变。体外研究显示BGM1962对AMY1R的激动活性远高于CTR,显著降低了脱靶风险;在体内药效模型中,BGM1962表现出显著的体重控制与摄食抑制作用;且其药代动力学特征优势突出。而在食蟹猴模型中,其半衰期长达约200小时,这种“每月一次”的极致低频给药潜力,能确保血药浓度在长周期内维持稳定,有效避免了浓度波动带来的不适感。这种对标全球顶尖PK数据(药代动力学数据)的表现,将为肥胖患者提供更具优势、更符合现代生活节奏的临床新选择。
前沿布局:siRNA技术开启低频给药新纪元
博瑞医药最惊艳的跨代布局,是处于PCC(临床前候选化合物)阶段的ALK7靶向siRNA项目。本产品拟用于超重/肥胖适应症,未来计划与GLP-1类药物联用以提升治疗效果。siRNA(小干扰RNA)作为一种前沿的基因沉默技术,其核心逻辑在于从分子源头“关掉”致病蛋白的表达。
该候选分子采用了行业顶尖的脂肪靶向递送技术,实现了组织特异性递送。通过精准下调ALK7基因,该项目能直接调节脂肪细胞的代谢平衡,减少脂肪堆积并改善胰岛素敏感性,这与传统药物单纯通过中枢抑制食欲的路径完全不同。
这一技术路径直接对标全球基因疗法领军企业Alnylam与再生元(Regeneron)合作的减重siRNA管线。 临床前研究显示,单次皮下注射可在非人灵长类动物中实现对ALK7基因大于80%的高效抑制。这种极长的维持时间,使得该项目具备了低频给药的潜力。
在全球范围内,利用siRNA技术解决肥胖症仍处于极早期,博瑞医药的这一布局标志着其在基因沉默这一减重药最尖端赛道中,已与跨国药企并肩而行。相比于目前主流的每日或每周给药,这种类似“疫苗化”的管理方案将极大地降低长期慢病管理的心理门槛,有望为长期体重管理提供跨时代的创新解决方案。
差异化创新构筑“护城河”
博瑞医药此次公布的管线,呈现出明显的协同效应、互补深度与战略前瞻性。BGM0504作为“动力引擎”提供基础减重效能,MSTN环肽作为“补丁”保障肌肉健康,口服BGM1812极大地提升了日常场景下的患者接受度,而siRNA项目则以极低频的给药频次锚定长期管理。这种多维度的产品组合,使得博瑞医药能够针对不同职业背景、不同肥胖程度以及不同依从性偏好的群体,提供个性化、闭环式的治疗矩阵,从而覆盖了从“起效”到“维持”再到“长期管理”的全生命周期。
业内专家认为,博瑞医药并未盲目跟风已陷入“红海”的传统单靶点减重药,而是通过对Amylin、GDF8、ALK7等前沿靶点的深度挖掘,构建了一个兼顾减重质与量的全方位“护城河”。这种差异化布局不仅能有效对冲单一靶点药效边际递减的风险,更向资本市场清晰展示了其作为全球代谢药物创新“第一梯队”的硬核实力。随着这些管线由临床前迈向临床阶段,博瑞医药正在完成从“跟随式创新”向“引领式创新”的跨越,有望在全球万亿规模的减重市场中重塑中国药企的估值标杆。


