华东医药股份有限公司(证券简称“华东医药”,000963.SZ)在创新药领域的持续投入迎来了收获期。公司近日发布的半年报显示,今年上半年,公司实现营业收入216.75亿元,同比增长3.39%;归属于上市公司股东的净利润18.15亿元,同比增长7.01%;归属于上市公司股东的扣除非经常性损益的净利润17.62亿元,同比增长8.40%。其中,公司创新产品业务收入当期同比增幅达59%,占医药工业整体收入的比重已接近15%,随着创新产品收入的快速增长,其整体占比也将进一步提升。华东医药在本年度中期拟向全体股东每10股派发现金红利3.50元(含税),共分红6.14亿元。
创新产品表现亮眼 医美板块业绩承压
华东医药创建于1993年,总部位于浙江杭州,2000年1月在深圳证券交易所上市。历经30余年的发展,公司业务覆盖医药全产业链,拥有医药工业、医药商业、医美、工业微生物四大业务板块,已发展成为集医药创新研发、生产、经销为一体的大型综合性医药上市公司。2020年,受集采政策等因素影响,华东医药业务遭受重创,当年营收出现负增长,2021年—2023年,公司砍掉非核心资产,重仓创新药、医美等,营收重回增长态势。
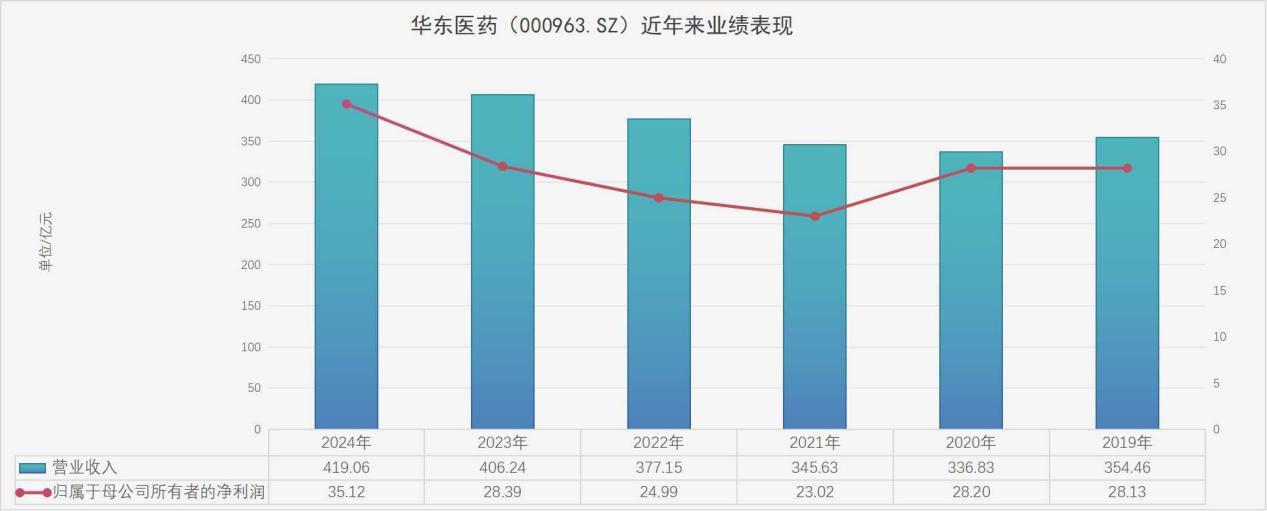
图:华东医药近年来业绩表现(单位/亿元) 数据来源:Wind 制图:郭新志
分业务板块来看,华东医药今年上半年四大业务板块业绩分化明显。
医药工业方面,核心子公司中美华东实现营业收入73.17亿元,同比增长9.24%;归属于上市公司股东的净利润15.80亿元,同比增长14.09%。报告期内,公司医药工业商业化创新产品梯队持续扩容,已覆盖肿瘤、内分泌、自身免疫等多个重点治疗领域。报告期内,受益于新产品陆续获批上市带来的增量释放,创新产品业务收入贡献持续攀升,当期实现销售及代理服务收入合计10.84 亿元,同比增幅达 59%,已进入高速增长通道,成为医药工业持续增长的核心驱动力之一。
医药商业板块整体继续保持稳健发展,报告期内实现营业收入139.47亿元,同比增长2.91%,实现净利润2.26亿元,同比增长3.67%,增速略显平淡,公司表示,上半年面临支付端控费深化与市场结构性调整的双重压力。
工业微生物板块,报告期内各业务单元均保持较快增长,整体销售趋势持续向好,合计实现销售收入3.68亿元,较去年同期增长29%。其中,特色原料药&中间体板块增长23%,xRNA板块增长37%,大健康&生物材料板块增长21%,动物保健板块增长超过100%。
医美板块,在市场需求调整等外部压力下,医美行业增长步入阶段性承压期。报告期内公司医美板块合计营业收入达到11.12亿元(剔除内部抵消因素),同比下降17.50%。其中,全资子公司英国Sinclair实现销售收入约5.24亿元,同比下降7.99%;国内医美全资子公司欣可丽美学实现营业收入5.43亿元,同比下降12.15%。
加大三大领域研发投入 内分泌在研管线进展顺利
研发方面,2025年上半年,华东医药工业研发投入(不含股权投资)14.84亿元,同比增长33.75%,其中直接研发支出11.74亿元,同比增长54.21%,直接研发支出占医药工业营收比例为15.97%。
目前,华东医药创新药研发中心正在推进80余项创新药管线研发。公司创新药研发中心正在推进80余项创新药管线研发。适应症布局上,主要集中在内分泌、自身免疫及肿瘤领域,同时向心血管、肾脏疾病等领域拓展。新品种的立项时会优先考虑first-in-class或best-in-class的产品。
肿瘤领域,主要围绕ADC进行布局。靶向MUC17的HDM2012已获得中国和美国的IND批准,用于治疗晚期实体瘤的中国Ⅰ期临床试验于2025年8月完成首例受试者给药;靶向FGFR2b的HDM2020已获得中国和美国的IND批准,用于治疗晚期实体瘤的中国Ⅰ期临床试验于2025年8月完成首例受试者给药;靶向CDH17的HDM2017已于2025年7月完成中国IND递交;双靶点ADC HDM2024正有序推进临床前研究,预计于2025年第四季度提交IND申请。
自身免疫领域,first-in-class双特异性抗体候选药物HDM3018注液正在进行IND开发工作,预计2026年第三季度前获得中国和美国的IND批件,拟开发适应症为炎症性肠病(IBD)、斑块状银屑病(PsO)及银屑病关节炎(PsA);first-in-class双特异性抗体候选药物HDM4002注射液正在进行IND开发工作,预计2026年第三季度前完成中国和美国IND申报,拟开发适应症为IGA肾病。HDM4002预计将于今年11月在美国肾脏病学会(ASN)大会做Post展示。
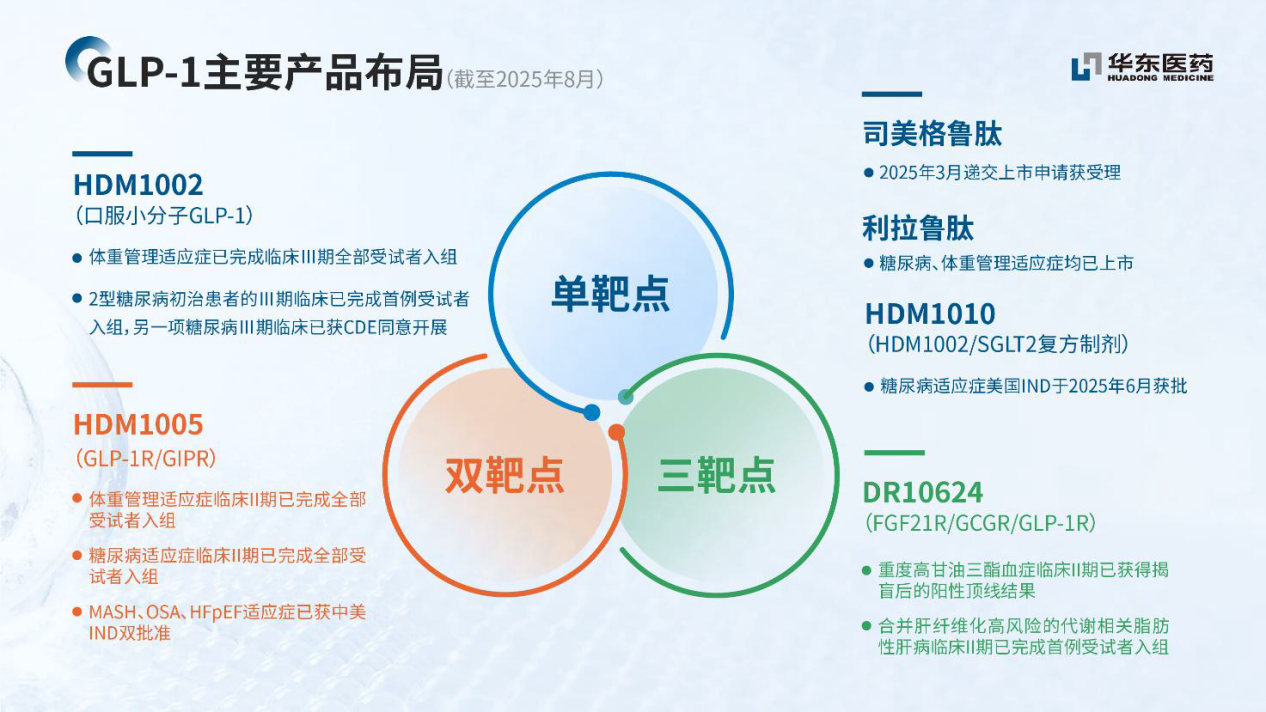
图:华东医药GLP-1主要产品布局 资料来源:公司2025半年报
内分泌领域,公司的研发主要围绕GLP-1靶点进行布局。口服小分子GLP-1受体激动剂HDM1002(conveglipron),目前已完成体重管理适应症中国临床Ⅲ期研究的全部受试者入组。此外,该产品用于2型糖尿病初治患者的Ⅲ期临床研究已完成首例受试者入组,另一项糖尿病适应症Ⅲ期临床研究已获CDE同意开展;GLP-1R/GIPR双靶点长效多肽类激动剂HDM1005(poterepatide),目前正在开展体重管理适应症Ⅱ期临床试验,已于2025年4月完成Ⅱ期全部受试者入组,预计2025年第四季度进入Ⅲ期临床研究。此外,糖尿病适应症Ⅱ期临床试验已于2025年7月完成全部受试者入组;FGF21R/GCGR/GLP-1R三靶点激动剂DR10624,已成功完成重度高甘油三酯血症的Ⅱ期临床研究并获得揭盲后的阳性顶线结果。此外,合并肝纤维化高风险的代谢相关脂肪性肝病以及代谢合并酒精相关脂肪变性肝病的Ⅱ期临床研究,于2025年4月完成首例受试者入组;HDM1010片(HDM1002固定比例复方口服制剂)2型糖尿病适应症的IND申请已于2025年6月获得美国FDA批准,目前已经启动临床准备工作;司美格鲁肽注射液糖尿病适应症的上市申请已于2025年3月递交并获受理;体重管理适应症已于2025年2月完成Ⅲ期临床研究全部受试者入组,预计2025年第四季度获得顶线结果。
财报显示,截至今年6月末,华东医药应收账款达91.30亿元,同比增长14.63%,占营业收入的比例升至43%。应收账款周转天数则从2024年上半年的66.20天增加至本期的72.90天,资金回收效率呈现下滑趋势。同时,公司期末存货达50.30亿元,同比增长14.85%,存货周转天数由去年上半年的55.30天增加至本期的61.60天。其中库存商品期末账面价值38.66亿元,同比增长27%,本期存货跌价准备计提1701.09万元,计提规模接近去年全年水平。
8月22日,华东医药收于45.63元/股,跌幅0.18%。(实习生马金戈对本文亦有贡献)


